Lääkkeiden saatavuudesta pidetään huolta
Teksti: Heli Selin, toimittaja
Viime vuosien tapahtumat maailmalla ja Euroopassa ovat lisänneet kansalaisten epävarmuuden tunteita. Suomi varautuu mahdollisiin kriiseihin turvaamalla huoltovarmuutta, jolla varmistetaan, että yhteiskunnan kriittiset toiminnot ja ihmisten arki jatkuisivat mahdollisimman normaalisti myös poikkeusoloissa. Lääkkeiden saatavuudesta huolehtiminen on yksi tärkeä osa terveydenhuollon huoltovarmuutta.
Lääkkeiden saatavuushäiriöt ovat lisääntyneet niin Suomessa kuin muuallakin Euroopassa. Suomi on riippuvainen lääkkeiden maahantuonnista, sillä valtaosa lääkkeistä valmistetaan ulkomailla. Lääkeyrityksien tehtävänä on varmistaa, että Suomessa markkinoilla olevaa myyntiluvallista lääkettä on riittävästi saatavilla. Lääkealan turvallisuus- ja kehittämiskeskus Fimea turvaa lääkehuoltoa ja varmistaa lääkkeiden saatavuuden maahan. Fimean ylitarkastajan Tarja Sissala-Airaksisen mukaan saatavuushäiriöistä on tullut uusi normaali.
”Seuraamme koko ajan näin normaalioloissakin lääkkeiden saatavuustilanteita ja reagoimme tarvittaessa. Mikäli esimerkiksi useammasta kilpirauhaslääkkeestä ilmenisi saatavuushäiriöitä, olisimme yhteydessä myyntiluvan haltijoihin ja alkaisimme selvittää tilannetta.”
Sissala-Airaksisen mukaan Suomessa voidaan olla rauhallisin mielin lääkkeiden riittävyyden suhteen. Saatavuushäiriöt eivät ole kovin pitkiä ja useimmat valmisteet ovat korvattavissa. Myös Fimean koordinoiva ylilääkäri Kari Syvänen suhtautuu lääkkeiden riittävyyteen turvallisin mielin. Jos myyntiluvallisella lääkevalmisteella on saatavuushäiriötä, voidaan harkita erityis- tai poikkeuslupamenettelyjä saatavuuden ja lääkehoitojen jatkuvuuden turvaamiseksi.
”Saatavuushäiriöiden myötä nämä mekanismit ovat toiminnassa näin normaalioloissakin, eikä niitä tarvitse enää myöhemmin käynnistää.”
Tyroksiinilla hyvät varastot
Suomessa lääkkeiden huoltovarmuutta parantaa olennaisesti lääkkeiden velvoitevarastointilaki, jonka piiriin tyroksiini elintärkeänä lääkkeenä kuuluu. Lain mukaan tyroksiinia tulee olla varastoituna kuuden kuukauden normaaliajan kysyntää vastaava määrä. Lääkkeiden varastointivelvollisia ovat mm. Suomessa toimivat lääketehtaat, lääkkeiden maahantuojat ja terveydenhuollon toimintayksiköt.
Tyroksiinivalmistetta maahantuovan Orion Pharman maajohtaja Janne Maksimainen pitää velvoitevarastointia tyroksiinin huoltovarmuuden kannalta hyvin positiivisena asiana, ja korostaa, että kaikki lääkkeiden velvoitevarastot sijaitsevat Suomessa.
Toista tyroksiinilääkettä maahantuovan Vermanin aluepäällikkö Janne Kovalainen kertoo, että velvoitevarastointi käsittää kaikki heidän valmisteensa 13 eri vahvuutta, joita Suomessa myydään.
Molemmilla lääkeyhtiöillä on myös kaupallisia lääkkeiden käyttövarastoja, joita ei lasketa osaksi velvoitevarastoja. Kovalaisen mukaan tuotteen hyvä säilyvyys mahdollistaa suuret käyttövarastot.
”Meillä on tyroksiinia normaalistikin isot erät tukussa, koska lääkkeen säilyvyys on tällä hetkellä kolme vuotta ja käyttäjiä on paljon. Jos näkisimme, että poikkeustila on tulossa, tilaisimme tuotetta mahdollisimman suuret määrät, jotta varastot riittäisivät pitkään.”
Myös apteekeilla on merkittävä rooli lääkkeiden huoltovarmuuden turvaamisessa. Jokaisella apteekilla on lakisääteinen velvollisuus varastoida vakiintuneen asiakaskunnan kahden viikon tarvetta vastaava määrä lääkkeitä.
Suomen laaja apteekkiverkko on rakennettu siten, että apteekit olisivat helposti saavutettavissa kaikkien kansalaisten osalta myös haja-asutusalueilla. Maksimainen näkisi tärkeänä, ettei apteekkien toimintaedellytyksiä enää heikennettäisi uusilla leikkauksilla, jotta ne eivät johtaisi apteekkiverkoston harvenemiseen ja sitä kautta lääkkeiden huoltovarmuuden heikkenemiseen.
Suomi riippuvainen maahantuonnista
Suurin osa Suomessa käytettävistä lääkkeistä valmistetaan maamme rajojen ulkopuolella. Molempien lääkeyhtiöiden tyroksiinivalmisteet ja niiden vaikuttavat lääkeaineet valmistetaan kuitenkin Euroopan unionin alueella, eikä niillä ole ollut saatavuuden kannalta ongelmia.
Yleisesti ottaen Eurooppa on kuitenkin hyvin riippuvainen maahantuonnista, etenkin vaikuttavien lääkeaineiden osalta. Maksimaisen mukaan lääkkeiden hintakilpailu on johtanut siihen, että lääkkeiden valmistus on siirtynyt Kiinaan ja Intiaan edullisempien tuotantokustannusten takia. Orionilla on yhä Suomessa merkittävästi lääkevalmistuskapasiteettia kuuden lääketehtaan myötä, mutta kaikkia valmisteita, esimerkiksi rokotteita, ei pystytä valmistamaan kotimaassa.
Lääkkeiden hintojen laskun voidaan ajatella hyödyttävän kansalaisia ja pienentävän yhteiskunnan maksamia lääkekorvauksia. Eniten saatavuushäiriöitä on kuitenkin havaittu olevan viitehinnaltaan alle 10 euron lääkkeillä. Maksimainen on huolissaan uusista suunnitteilla olevista leikkauksista, jotka halpoihin tuotteisiin kohdistuessaan voisivat myös vaikuttaa edullisen tyroksiinin saatavuuteen.
”Kustannukset nousevat jo inflaation myötä kaikilla lääkeketjun toimijoilla, mikä muodostaa haasteen sille, kuinka kannattavaa lääkkeitä on valmistaa Euroopassa tai Suomessa. Lääkkeet ovat välttämättömyyshyödykkeitä ja päättäjien tulisi pikemminkin tukea alan toimintaedellytyksiä, eikä kohdistaa sinne leikkauksia.”
Lääkkeiden toimitusketju voi olla hyvinkin pirstaloitunut ympäri maailmaa. Tämä heikentää lääkkeen saatavuutta ja pienikin häiriö toimitusketjun jossain osassa voi aiheuttaa saatavuushäiriöitä. Lääkkeiden logistiikkaketju, alkaen raaka-ainekemikaalien valmistuksesta, voi olla hyvin pitkä, jopa 12 kuukautta. Maksimaisen mukaan tyroksiinin saatavuutta parantaakin sen vuodesta toiseen hyvin ennustettavana pysyvä tarve. Lääkkeillä, joilla on vaihteleva kysyntä, on heikompi huoltovarmuus. Kovalainen muistuttaa myös, että tyroksiinilla on suuri käyttäjäkunta, mikä parantaa lääkkeen saatavuutta.
”Tyroksiinia käyttäviä potilaita on paljon ja lääkkeitä tulee meille jatkuvasti. Isommat riskit liittyvät lääkkeisiin, joilla on vähän käyttäjiä.”
Lääkehuoltovarmuutta yhteistyöllä
Koronapandemian aikana lääkkeiden velvoitevarastot osoittivat hyödyllisyytensä, kun niiden avulla pystyttiin huolehtimaan kriittisten lääkkeiden saatavuudesta Suomessa. Maksimaisen mukaan lääkkeiden käyttö- ja velvoitevarastot ovat suuri apu lyhytaikaisempiin kriiseihin. Pidempiaikaisissa poikkeusoloissa lääkevarastojen avulla pystytään ostamaan lisää aikaa, jotta mahdollisiin saatavuusongelmiin ehdittäisiin löytää ratkaisuja.
”Korona-aika ja Venäjän hyökkäyssota Ukrainaan ovat osoittaneet, että moni aiemmin varmana pidetty asia on muuttunut. Toisaalta positiivista on, että olemme nyt paremmin varautuneita, kun asioita ei enää pidetä itsestäänselvyyksinä.”
Vuosia kestävissä poikkeusoloissa olisi Maksimaisen mukaan tärkeää varmistaa, että logistiikka Suomeen olisi turvattu useampaa reittiä pitkin. Tämänhetkiseen tehdaskapasiteettiin peilaten Maksimainen ei pidä teknisesti mahdottomana ajatusta siitä, että tyroksiinia voitaisiin valmistaa myös Suomessa, jos lääkkeen tulo maahan olisi huomattavasti vaikeutunut. Maksimaisen mukaan kapasiteettia tulisi tällöin vapauttaa muilta valmisteilta ja kustannustason haasteet tulisi voida ratkaista. Positiivinen puoli tyroksiinin valmistuksessa olisi vähäinen vaikuttavan aineen tarve.
”Yksi tabletti sisältää mikrogrammoja vaikuttavaa ainetta ja mikrogramma on tuhannesosa milligrammasta, joten ei puhuta valtavasta määrästä vaikuttavaa ainetta, jota tarvittaisiin maahan kuljetettavaksi.”
Syväsen mukaan muuallakin Euroopassa ollaan korona-ajan ja Ukrainan tilanteen myötä havahduttu siihen, että Euroopan täytyy kehittää mekanismejaan, joilla kriittisten lääkkeiden saatavuus voidaan turvata. Fimea tekee aktiivista yhteistyötä lääkealan toimijoiden ja muiden Euroopan lääkeviranomaisten kanssa lääkkeiden saatavuuden parantamiseksi. Sissala-Airaksinen korostaa myös Pohjoismaisen yhteistyön tärkeyttä, ja sitä, että Suomessa tehdään koko ajan töitä kaikkien lääkkeiden saatavuuden ja huoltovarmuuden turvaamiseksi.
”Meillä työskentelee osaavia ihmisiä lääkkeiden saatavuuden parissa”, Sissala-Airaksinen rauhoittelee.
Maksimainen ymmärtää, että viimeaikaiset maailman tapahtumat ovat voineet herättää huolen lääkkeiden riittävyydestä, mutta korostaa, että akuuttia hätää ei ole.
”Luottavaisin mielin yhdessä eteenpäin, se on kaikista tärkeintä. Teemme kaikissa olosuhteissa, niin normaaliaikoina kuin erityisesti, jos olisimme poikkeusolosuhteissa kaikkemme, että tyroksiinia olisi saatavilla.”
Lähteet: Fimea, huoltovarmuuskeskus.fi
Saatavuushäiriötilanteessa
- Apteekki voi tarkistaa, löytyykö tarvitsemallesi lääkkeelle vaihtokelpoista valmistetta.
- Voit etsiä apteekki.fi -sivujen lääkehakupalvelusta lähimmän apteekin, jossa lääkettä on saatavilla.
- Voit tarkistaa saatavuushäiriön keston Fimean saatavuushäiriöhausta. Jos lääke ei näy saatavuushäiriöhaussa, jätä viesti Fimeaan, joka selvittää asiaa lääkeyrityksen kanssa.
- Tarvittaessa lääkäri voi määrätä korvaavan lääkkeen. Jos reseptilääkkeesi uhkaa loppua saatavuushäiriön aikana, ole yhteydessä hoitavaan lääkäriin korvaavan hoidon selvittämiseksi.
- Kilpirauhasliitto tiedottaa verkkosivuillaan ja sosiaalisen median kanavillaan tiedossa olevista saatavuusongelmista kilpirauhaslääkkeiden osalta.
Lähteet: Fimea.fi, Kilpirauhasliitto
Velvoitevarastointilaki
- turvaa elintärkeiden lääkkeiden saatavuuden ja käyttömahdollisuudet tilanteissa, joissa lääkkeiden saanti Suomeen vaikeutuu tai estyy esimerkiksi toimituskatkosten, vakavan kriisin tai muun näihin verrattavan syyn vuoksi
- koskee ensisijaisesti valmisteita, joilla turvataan elintärkeä lääkehoito sekä laajan yleiskirurgian ja tehohoidon toiminta
- määrää eri lääkeryhmien velvoitevarastointien pituudet; tyroksiinivalmisteita tulee olla velvoitevarastoissa 6 kk normaalikulutusta vastaava määrä
- koskee lääketehtaita, lääkkeiden maahantuojia, terveydenhuollon toimintayksiköitä ja THL:ää
- määrää, että velvoitevarastojen on sijaittava
Poikkeuslupa
- haetaan myyntiluvanhaltijan toimesta ja sen myöntää Fimea
- voidaan myöntää esimerkiksi, jos lääkehuollolle kriittisen valmisteen saatavuudessa on odotettavissa katkos, eikä korvaavaa valmistetta ole, tai lääkkeen kysyntä on odottamattomasti kasvanut
- turvaa lääkehoitoa tilanteissa, joissa on tarpeen poiketa lääkevalmisteen myyntiluvan ehdoista, jolloin Fimea voi myöntää luvan tuoda Suomeen esim. vieraskielisiä pakkauksia.
Erityislupa
- voidaan hakea Fimealta hoitavan lääkärin toimesta lääkevalmisteelle, jolla ei ole myyntilupaa Suomessa
- myönnetään, jos lääkäri katsoo, ettei hoitoon ole muuta valmistetta saatavilla tai tarjolla lääkkeet ovat epäsopivia kyseisen potilaan hoitoon, eikä niillä saavuteta toivottua tulosta
- haetaan lääkärin laatimalla erityislupahakemuksella, jonka potilaan valitsema apteekki toimittaa Fimeaan käsiteltäväksi
- on potilaskohtainen, maksullinen ja voimassa yhden vuoden
- voidaan poikkeustapauksissa myöntää myös itse Fimean toimesta määräaikaisena erityislupana. Tätä hyödynnettiin esimerkiksi koronapandemian aikana, jolloin terveydenhuollon potilaskontakteja oli perusteltua rajoittaa.
Lähde: Fimea

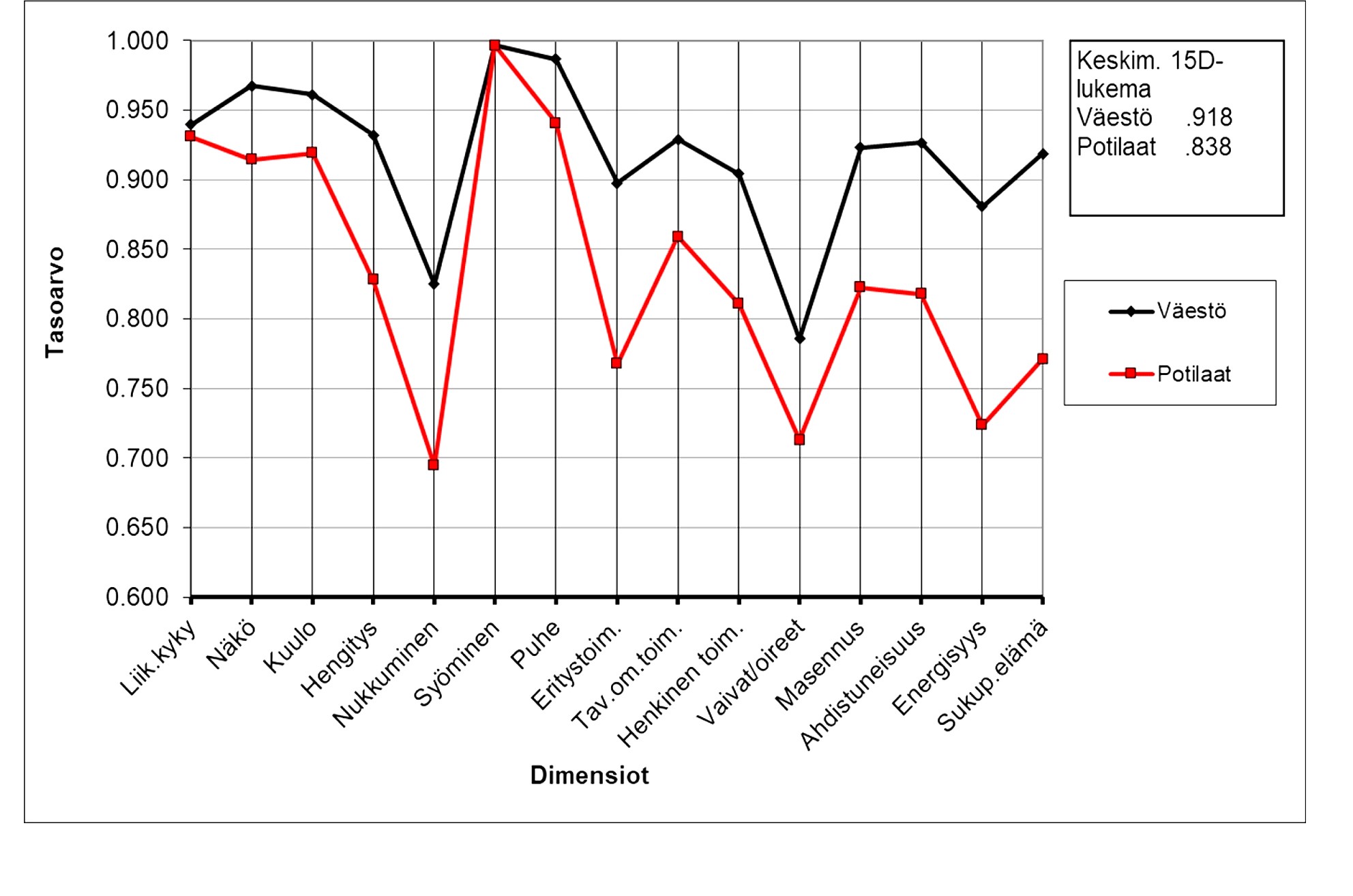 Kuva. Kilpirauhasen vajaatoimintaa sairastavien (punaisella) ja heidän kanssaan ikä- ja sukupuolivakioidun väestön (mustalla) keskimääräinen 15D-profiili ja -kokonaislukema (15D-score).
Kuva. Kilpirauhasen vajaatoimintaa sairastavien (punaisella) ja heidän kanssaan ikä- ja sukupuolivakioidun väestön (mustalla) keskimääräinen 15D-profiili ja -kokonaislukema (15D-score).
 Lähteet: 22q11 Finlandin kautta
Lähteet: 22q11 Finlandin kautta
